Чужие среди своих
Поросята с изюминкой
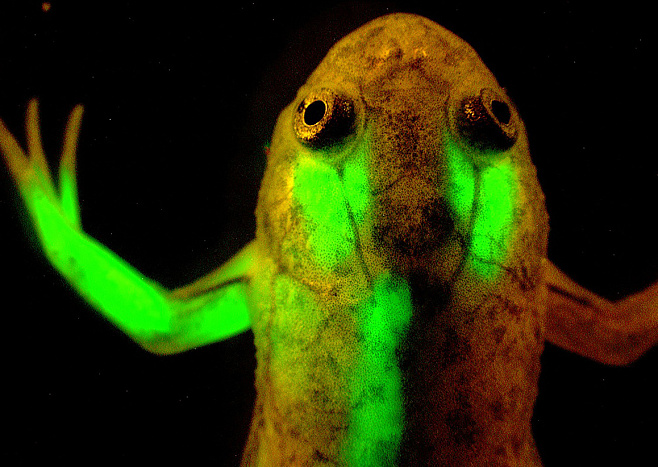
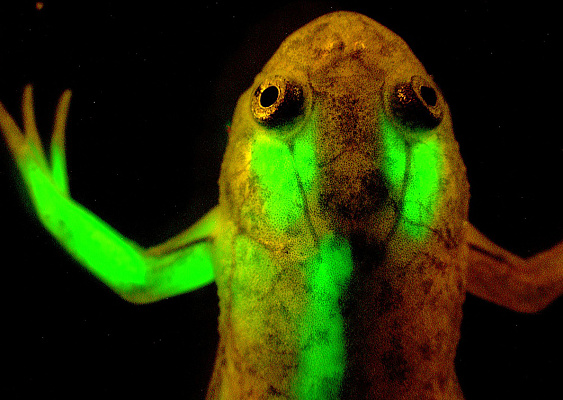
Зеленоватый поросенок, который светится ярким неоновым цветом, – звучит как чудо из сказки? Нет, это всего лишь результат генных экспериментов. Исследователи из Национального университета Тайваня во главе с профессором У Шинь-Чжи в январе 2006 года сообщили научному миру о своих трансгенных свиньях.
Трех самцов вывели так: в ДНК-цепочку эмбриона ввели ген зеленого флуоресцентного белка (GFP), взятого у медузы Aequorea victoria. Такие эмбрионы ученые имплантировали в матки восьми самок. Только четыре из них забеременели, а у трех успешно родились поросята зеленоватого оттенка, которые светятся неоново-салатовым цветом, если направить на них ультрафиолетовые лучи. Шинь Чжи подчеркивает, что главное отличие этих свиней от других трансгенных – в том, что даже их органы зеленого цвета.
Это не первый такой эксперимент над животными – подопытными генетиков становились и мыши, и рыбки, и кошки, и собаки. Внедрив GFP (или похожие на него белки) в организм и связав его с другими белками, можно изучать их работу в организме, определить, где именно внутри клетки они находятся, не потревожив при этом саму клетку.
 Зеленоватые поросята с GFP в цепочке ДНК. foreignerinformosa. typepad.com
Зеленоватые поросята с GFP в цепочке ДНК. foreignerinformosa. typepad.com Кот по имени Мистер Зеленые гены – первое флуоресцентное животное из семейства кошачьих. telegraph.co.uk
Кот по имени Мистер Зеленые гены – первое флуоресцентное животное из семейства кошачьих. telegraph.co.uk
В середине XX века американских фермеров и крупные сельскохозяйственные предприятия одолели насекомые. Мясные мухи заражали скот: паразиты откладывали яйца в ранах животных, из которых вскоре вылуплялись личинки и питались плотью. Взрослую корову они могли убить за две недели! На помощь животным и людям, как супергерои из блокбастеров, поспешили энтомологи Рэймонд Бушлэнд (Raimond Bushland) и Эдвард Ниплинг (Edward Knipling). Только вооружились не суперспособностями и латексными костюмами, а биологией и рентгеновским аппаратом.
Их идею в научном мире встретили скептицизмом, и на полевых станциях в Техасе и Флориде они проводили исследования вопреки насмешкам коллег. А идея заключалась в том, чтобы стерилизовать мух. Бушлэнду и Ниплингу удалось поймать большое количество особей и облучить их рентгеновскими лучами для стерилизации. После этого их выпустили на волю, что просто-напросто остановило рост популяции насекомых-паразитов. Фермеры вздохнули спокойно. В 1958 году мясные мухи исчезли во Флориде, к 1960-му на всем юго-западе США, и в 80-х этот метод применялся уже во всей стране – от мух избавились. Спустя годы, в 1992-м, Ниплинг и Бушлэнд получили Всемирную продовольственную премию за свою работу.
 Стерилизованный самец мухи, помеченный для наблюдения. Фото: Peggy Greb/US Department of Agriculture, entomologytoday.org
Стерилизованный самец мухи, помеченный для наблюдения. Фото: Peggy Greb/US Department of Agriculture, entomologytoday.org
Технология стерилизации насекомых, или SIT (sterile insect technique), используется и сейчас. Например, британская компания Oxitec стерилизует комаров вида Aedes aegypti, которые переносят вирус-провокатор лихорадки денге. Только использует уже кое-что помощнее – генную модификацию. Ученые внедрили в геном насекомых ген tTAV, вызывающий быструю смерть – через два дня. После этого их отправили восвояси, чтобы те спаривались с самками и передавали своему потомству летальный ген.
В 2010 году Oxitec отправила ГМО-комаров на волю в пригороде Жуазейру (Бразилия). Даже за два дня жизни самцы успели произвести обреченное потомство – по данным мониторинга, через год их дикая популяция сократилась на 88 %. В 2020 году власти штата Флорида в США тоже дали компании добро на выпуск 750 млн комаров, и спустя год их выпустили. Сейчас ученые ждут результат. Британские биотехнологи не сомневаются, что смогут окончательно свести счеты с комариной популяцией и покончить с лихорадкой.
 У комара «вставлен» флуоресцентный красный маркер. Благодаря ему исследователям легче отслеживать особь. facebook.com/oxitec
У комара «вставлен» флуоресцентный красный маркер. Благодаря ему исследователям легче отслеживать особь. facebook.com/oxitec Трансгенные комары Oxitec вылетают из контейнера в Пирасикабе, Бразилия. Фото: PAULO FREIDMAN, sciencemag.org
Трансгенные комары Oxitec вылетают из контейнера в Пирасикабе, Бразилия. Фото: PAULO FREIDMAN, sciencemag.org
Я и четыре моих клона
Опять же азиатские ученые, сотрудники лаборатории Института нейронаук Шанхая (Китай) в 2019 году вывели пять клонированных обезьян с идентичными измененными генами. Они станут основой для исследований нарушений циркадных ритмов.
Для начала биотехнологам пришлось вывести генетически модифицированных макак без гена BMAL1. После одну из них клонировали. Из 325 эмбрионов получилось только пять клонов – все без гена BMAL1. Он регулирует работу циркадных ритмов: если его нет, то у особи ломаются режим сна и суточные ритмы, а это, в свою очередь, ведет к мигреням, депрессии, плохому самочувствию и нейровегетативным заболеваниям. Пятерых макак вывели, как раз чтобы изучать эти механизмы, – раньше для той же цели использовали мышей и мух. Согласитесь, между нами и мухами гораздо больше отличий, чем между нами и приматами. Поэтому исследования на клонированных обезьянах ускорят изучение механизмов циркадных ритмов и болезней, связанных с их нарушениями, а также методов лечения.
Ученые из Института нейронаук Шанхая планируют развивать свою технологию, чтобы в будущем клонировать макак с разными нарушениями и генетическими заболеваниями. По их мнению, это позволит уменьшить количество здоровых обезьян, используемых в опытах во всем мире.
 Пять клонированных макак, english.cas.cn
Пять клонированных макак, english.cas.cn
Непорочное зачатие
Для начала небольшой ликбез по зарождению жизни. Некоторые животные (например, ящерицы, рыбы, насекомые) могут самооплодотворяться – две их яйцеклетки сливаются и образуют зародыш. Среди млекопитающих это непопулярный метод размножения – у нас нет ни одного вида, самки которого могут обеспечивать себя потомством. Конечно, ученым давно хотелось обмануть природу и запустить процесс партеногенеза (самооплодотворения) искусственно. Но все как-то не получалось. До 2018 года.
Тогда китайские ученые из Института зоологии КАН в Пекине впервые объединили две яйцеклетки мышей, запустив развитие эмбрионов, которые в итоге стали здоровыми детенышами. Глава исследовательской группы Чжикунь Ли и его команда отыскали участки ДНК, мешающие запуску программы развития эмбриона, и научились «склеивать» пары яйцеклеток. С помощью наблюдения за стволовыми клетками ученые смогли создать «заготовки» мужских и женских половых клеток, лишенные родительских меток. Часть из них попытались объединить с обычными яйцеклетками и вырастить потомство в утробе суррогатных матерей.
Полученных зародышей имплантировали в матку самки. 14 % зародышей прошли все фазы развития, и вскоре у мамы родилось 30 мышат, не имеющих отца. Треть из них даже спарилась с обычными самцами и дала жизнь уже новому поколению.
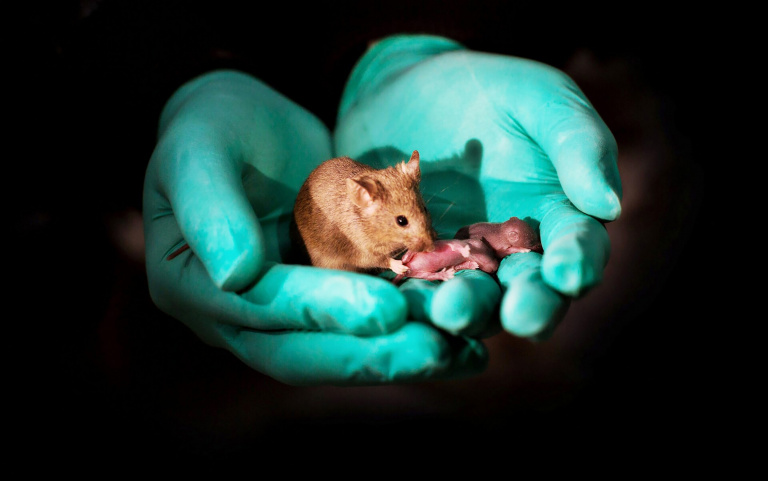 Мыши от двух матерей выросли до зрелого возраста и имели собственное потомство. Фото: Leyun Wang, scmp.com
Мыши от двух матерей выросли до зрелого возраста и имели собственное потомство. Фото: Leyun Wang, scmp.com
Не нуждающаяся в представлении
Самая известная овца в мировой истории – первое клонированное млекопитающее. В 1996 году Долли создали двое ученых, Ян Вилмут (Ian Wilmut) и Кит Кэмпбелл (Keith Campbell) из Рослинского института (Шотландия). Мир об этом узнал, только когда Долли было уже семь месяцев, – 22 февраля 1997 года. За это время исследователи оформили патент на технологию переноса ядра (Nuclear transfer).
Чтобы получить Долли, ядро взрослой соматической клетки пересадили в цитоплазму яйцеклетки, генетический материал которой был заранее удален. Прорыв этого эксперимента в том, что генетическую информацию для клонирования взяли не из половых или стволовых клеток, а из соматических. То есть, если у обычного живого организма есть генетические признаки отца и матери, то у Долли родитель был только один – овца-донор. Она к тому времени уже умерла, а часть ее клеток из вымени ученые сохранили, заморозив в жидком азоте. Их ядра эмбриологи перенесли в 277 яйцеклеток. Около 29 из них сумели развиться до эмбрионов, а выжил только один. Им и был ягненок, представленный миру как овечка Долли. Так ученые доказали, что клонирование теплокровных животных возможно, даже если они умерли, – главное, чтобы остался качественный генетический материал.
После Долли началась целая череда создания клонов – овец, коров, собак, обезьян, кроликов и других. А сама Долли прожила почти семь лет и родила шестерых ягнят. В 2003 году ее усыпили из-за долгой болезни.
 Овечка Долли со своим первенцем – ягненком Бонни. Фото: The Roslin Institute, The University of Edinburgh, nbcnews.com
Овечка Долли со своим первенцем – ягненком Бонни. Фото: The Roslin Institute, The University of Edinburgh, nbcnews.com
Коротко
Полина Агеева



 Крошечные боги: мифы и легенды о муравьях
Крошечные боги: мифы и легенды о муравьях Красная ртуть: легенда о красной материи
Красная ртуть: легенда о красной материи До самых корней
До самых корней Смотри, но не трогай
Смотри, но не трогай








