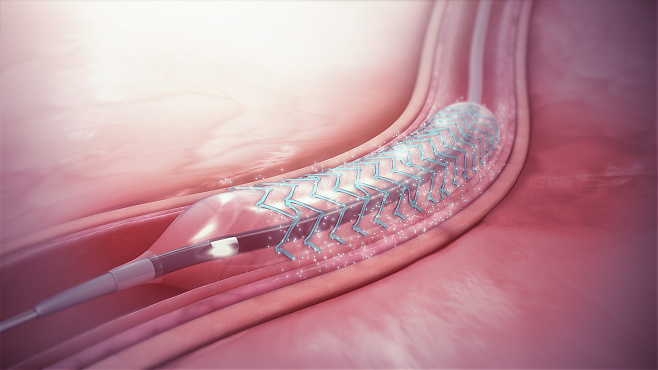
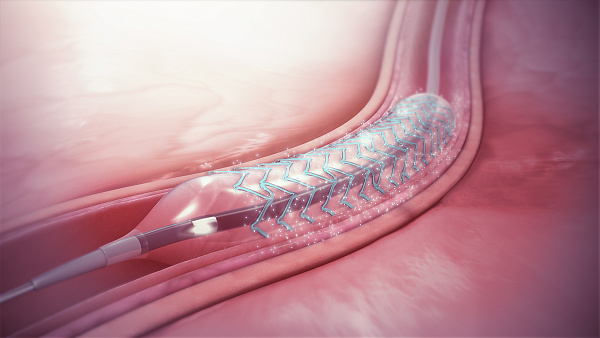
Ишемическая болезнь сердца — недуг, при котором миокард, или сердечная мышца, нуждается в большем количестве кислорода, чем поступает с кровью. Болезнь возникает из-за того, что на стенках коронарных артерий, оплетающих сердце, формируются бляшки, которые сужают их просвет и уменьшают кровоток. Для терапии чаще всего в место сужения устанавливают стент — своего рода каркас, который помогает восстановить прежний диаметр сосуда. Однако такое искусственное расширение может повредить стенку артерии, вызвать воспаление и разрастание ткани, а это повторно сузит просвет. Это осложнение называют рестенозом стента.
Кроме клинических исследований и экспериментов на модельных животных, для изучения механизмов рестеноза может использоваться компьютерное моделирование. Одной из распространенных является мультимасштабная модель рестеноза, а также ее двумерная версия. Модель состоит из трех подмоделей, которые имитируют стентирование и последующее сужение артерии. Она позволяет исследовать и анализировать процесс и выявлять его причины, но, в то же время, происходящее в сердце оказывается гораздо сложнее, а потому точность может быть недостаточной.
Ученые из Национального центра когнитивных исследований Университета ИТМО (Санкт-Петербург) и Амстердамского университета (Нидерланды) создали трехмерную вычислительную модель, которая воспроизводит сужение артерии после установки стента. В отличие от двумерной версии трехмерная моделирует патологию точнее. Она включила в себя три подмодели. Первая имитировала расширение артерии баллоном, которое осуществляют перед введением стента, а также саму установку конструкции; вторая воспроизводила биологическое и физическое состояние каждой клетки сосуда в месте установки стента; третья рассчитала то, как течет кровь. Авторы исследовали четыре параметра, которые потенциально могли вызывать сужение артерий: время регенерации внутренней поверхности сосуда, максимальное механическое напряжение, которое способны выдерживать клетки стенок, скорость кровотока и количество пор в эндотелии, выстилающем артерии изнутри.
На ранних этапах причиной развития патологии оказалось большое количество пор на внутренней поверхности артериальной стенки, то есть чем проще клеткам было попасть из внутренних слоев стенки сосуда в его просвет, тем сильнее сужение. На поздних и клинически значимых стадиях определяющими факторами стали время восстановления функции клеток поверхности сосуда и скорость кровотока, которая оказывала механическое воздействие на неизбежно повреждаемый при операции сосуд. Быстрое течение крови приводит к тому, что клетки выстилки сосуда начинают выделять вещества, которые подавляют клеточный рост, а вот при медленном кровотоке этого не происходило, клеточная масса продолжала расти, и артерия сужалась.
«Наш проект посвящен оценке неопределенности модели. Это необходимо для доверия к модели и в перспективе для возможности ее применения при разработке новых стентов. В дальнейшем мы хотим провести всесторонние исследования, чтобы ее можно было сертифицировать и применять в клинической практике. Конечная цель проекта — довести модель до такого состояния, когда ее можно будет задействовать непосредственно в расчетах рисков развития рестеноза для конкретного стента. Следующий шаг на пути к этому — валидация модели на клинических данных, над чем мы сейчас и работаем», — рассказал один из авторов Павел Зун, научный сотрудник Национального центра когнитивных разработок Университета ИТМО.
Результаты исследования, поддержанного
грантом Российского научного фонда (РНФ),
опубликованы в журнале Journal of the Royal Society Interface.


 Ученые нашли способ борьбы с атрофией скелетных мышц
Ученые нашли способ борьбы с атрофией скелетных мышц Реакторы для фотохимии будут печатать на 3D-принтере прямо в лаборатории и за один день
Реакторы для фотохимии будут печатать на 3D-принтере прямо в лаборатории и за один день








