Если я заменю батарейки
Покупаете предусмотрительно упаковку батареек, везете в отпуск, по приезде бежите фотографировать вечернюю набережную, а камера засыпает после нескольких снимков. Вы к мастеру, а он вам: «Так батарейки не подходят».
Да как не подходят?! Нормальные же батарейки, пальчиковые, как всегда. А надо было покупать вдумчиво, как продукты: не только название и размер проверить, но и состав.
До 1959 года все было проще: батарейки были только солевые, и оставалось лишь мириться с недостатками – которых у них, кстати сказать, немало. Например, маленькая емкость. В среднем емкость с


Покупаете предусмотрительно упаковку батареек, везете в отпуск, по приезде бежите фотографировать вечернюю набережную, а камера засыпает после нескольких снимков. Вы к мастеру, а он вам: «Так батарейки не подходят».
Да как не подходят?! Нормальные же батарейки, пальчиковые, как всегда. А надо было покупать вдумчиво, как продукты: не только название и размер проверить, но и состав.
До 1959 года все было проще: батарейки были только солевые, и оставалось лишь мириться с недостатками – которых у них, кстати сказать, немало. Например, маленькая емкость. В среднем емкость солевого элемента в 3–5 меньше, чем у щелочного (о них расскажем ниже), и это при малой и средней нагрузке. При высокой нагрузке (мощные фонари, фотоаппараты и видеокамеры) разница в емкости еще больше увеличивается и достигает 10. То есть солевая батарейка питает маломощный прибор, к примеру, 10 дней, а щелочная – 10 · 3 = 30 дней; такая же солевая батарейка обеспечит энергий фотоаппарат со вспышкой в течение 10 минут, а такая же щелочная – 10 · 10 = 100 минут.
Короткий срок хранения. У солевого элемента – 2 года, у щелочного – 7–10 лет. Правда, срок хранения солевой батареи можно увеличить, если держать ее в холодильнике: при низкой температуре химическая реакция, при которой происходит саморазряд, замедляется. Но для щелочных элементов температура хранения вообще некритична.
Узкий температурный диапазон эксплуатации. Солевые батареи отказываются работать при отрицательных температурах, а щелочная при –20 °С отдает такую же емкость, как солевая в режиме беспрерывного разряда при комнатной температуре.
В общем, к сегодняшнему дню у солевых элементов питания осталось только одно преимущество – низкая цена благодаря дешевизне реагентов и материалов. Да и технология их производства проста и вылизана до идеала уже давным-давно.
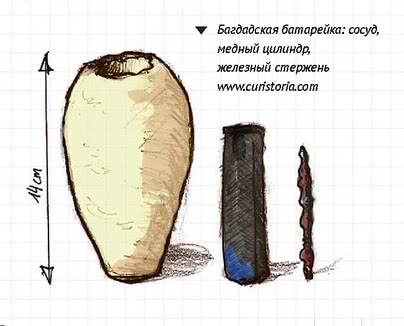
В последнее время археологи стали утверждать, что нечто похожее на химические источники тока появилось в Месопотамии за 100 лет до н. э. (так называемая Багдадская батарейка). Но это все на уровне гипотезы, а официальное рождение батареи относят к 1800 году, когда итальянский физик Алессандро Вольта, основываясь на опытах итальянского врача и анатома Луиджи Гальвани, сделал устройство, получившее впоследствии название «вольтов столб». Сложив полуметровую стопку из пластинок цинка, меди и войлока, смоченного раствором серной кислоты, Вольта приложил руки к концам стопки и получил весьма чувствительный удар током. Так началась электрическая эра. Изобретение произвело фурор в обществе, Вольта осыпали почестями, его именем назвали единицу электрического напряжения. Свою долю славы получил и Гальвани – в его честь электрохимический элемент, изобретенный Вольта, называется гальваническим (несколько парадоксально, конечно).

Что нам известно о гальваническом элементе из школьной программы? Что это источник электрического тока, основанный на химической реакции двух металлов (или их оксидов для удешевления/простоты использования). Один из металлов – анод – всегда более активный, чем второй – катод, и эти металлы помещены в токопроводящую среду – электролит. При соединении металлов проводником образуется электрическая цепь и начинает вырабатываться ток, который бежит от анода (–) к катоду (+).
Гальванические элементы делятся на первичные и вторичные. Первичные напрямую преобразуют химическую энергию, содержащуюся в реагентах, в электрическую энергию. Этот процесс идет до полного расхода реагентов, после чего выработка электричества прекращается. Проще говоря, это одноразовые элементы. Все батарейки являются первичными гальваническими элементами.
Во вторичных гальванических элементах электрическая энергия от внешнего источника тока превращается в химическую энергию и накапливается, а затем, при необходимости, химическая энергия снова превращается в электрическую. Вторичные элементы называются аккумуляторами, и эта обширная тема достойна отдельной большой статьи.
Один из первых гальванических элементов, которым можно было пользоваться вне лабораторий, изобрел Жорж Лекланше в 1866 году. Конструкция простая: цинковый анод и катод из диоксида марганца с углем, размещенные в электролите из хлорида аммония, то есть соли аммония. В течение некоторого времени элемент Лекланше изменился: цинковый анод стал делаться в виде стаканчика, в нем разместился катод из смеси диоксида марганца и графита, в центре катода находится угольный стержень – токосъемник, катод окружен электролитом из хлорида аммония с добавкой хлорида цинка – только не в жидком виде (как у Лекланше), а в загущенном, в виде геля (из-за добавления крахмала и муки). Это необходимо, чтобы электролит не мог вытечь или высохнуть при хранении и эксплуатации элемента. Элементы с таким загущенным электролитом получили название «сухие батареи».
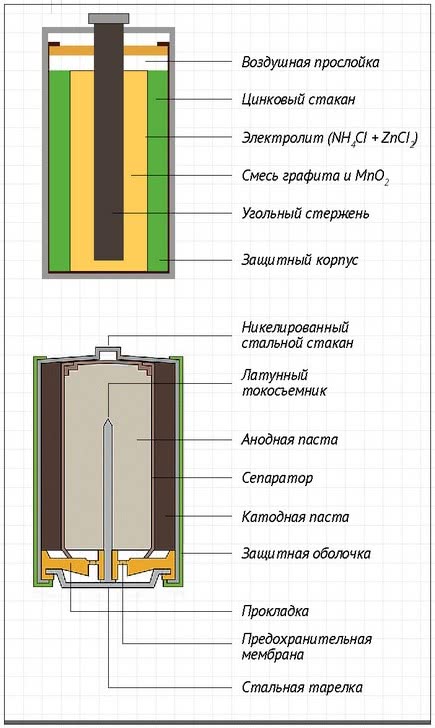
Такова классическая конструкция солевого гальванического элемента: по такой технологии он производится уже 150 лет. Получается как-то не очень хорошо с темпами развития науки в смежных областях. Пятитонный компьютер MARK-1 площадью 60 м2 за 60 лет уменьшился до микросхемы (с намного большими возможностями!) весом в доли грамма и размером с булавочную головку – и этот хайтек питает энергией древняя, двухсотлетняя технология! Печально. А что еще грустно: фирмы, выпускающие элементы питания, не испытывают никаких иллюзий насчет революционных технологий производства портативных источников тока и откровенно говорят, что в ближайшем и даже не очень ближайшем будущем нас ожидает только постепенное улучшение характеристик батарей – по полпроцента в год. Правда, всплески на ровном графике все же были – например, появление щелочных батарей.
Впервые щелочные (или алкалиновые) батарейки выпустила компания Eveready (ныне Energizer) – в том самом 1959 году. Принцип их работы практически идентичен с солевой батареей – анод из цинка, катод из диоксида марганца, единственное отличие – состав электролита: он не из соли аммония, а из раствора щелочи, обычно гидроксида калия. И конструкция отличается: она «вывернута наизнанку» по сравнению с солевым элементом. У того анод в виде цинкового стаканчика заполнен катодом в виде диоксида марганца, разделенным электролитом из соли аммония, а у щелочной батареи анод в виде пасты из цинкового порошка в смеси с электролитом находится внутри катода из смеси диоксида марганца с графитом. Анод и катод разделены тонким сепаратором, пропитанным электролитом, и все это располагается в стальном корпусе. Получается, что если у солевого элемента корпус (–), а центральный токоотвод (+), то у щелочного элемента все наоборот: корпус (+), а центральный токоотвод (–).
Такая конструкция, разумеется, сделана не просто так. Выше упоминалось, что первичные гальванические элементы преобразуют химическую энергию, содержащуюся в реагентах элемента. В солевых элементах при химической реакции расходуются все реагенты, его составляющие, – анод, катод, электролит. А в щелочном элементе при химической реакции расходуются только анод и катод. Поэтому электролита там совсем мало, и «освободившееся» место электролита заполнено увеличенным количеством анода и катода, что и способствует похвальной электроемкости щелочного элемента.
В последние несколько лет в продаже появился новый тип элементов – литиевый. Принцип действия похож на принцип солевого и щелочного элемента, но анод изготовлен из лития или его соединения. Литий имеет наивысший отрицательный потенциал по отношению к остальным металлам, соответственно, он имеет наибольшее номинальное напряжение при минимальных размерах. И другие параметры тоже превосходные: очень долгое время хранения (до 15 лет), исключительно малые токи саморазряда и высокая степень герметичности, хранение и работа в широком диапазоне отрицательных и положительных температур. Но цена! Литиевая пальчиковая батарейка может быть в шесть раз дороже алкалиновой и в 13 раз дороже солевой.

Выбирать элементы питания надо с учетом мощности приборов. Например, ваша «отпускная» фотокамера – прибор с большим потреблением тока и большими колебаниями энергии, для нее нужно покупать щелочные батарейки, а для телевизионного пульта пойдут солевые. Как отличить одни от других? Смотрите маркировку: на упаковке солевых батареек написано Normal или Standard, а щелочные обозначаются как Alkaline. А вот качество по картинке, увы, не определить. И по ценнику тоже. Мы привыкли выбирать элементы известных фирм, которые на слуху благодаря навязчивой рекламе, – а зря. Ведь рекламный бюджет надо отбивать, и расходы на рекламу включаются в цену товара. Две же обычные батарейки по емкости могут спокойно перекрыть одну супербатарейку. Энтузиасты выкладывают в Сеть тесты батареек различных фирм, посчитав комплексный параметр цена/емкость. Лидерами в таких тестах порой становятся безымянные элементы питания из гипермаркета, чей ватт мощности оказывается самым дешевым, оставив позади именитые фирмы.
За пределами статьи осталось много интересных элементов – воздушно-цинковые, ртутные, серебряные и т. д. Но все это – перепевы классического гальванического элемента, изобретенного почти 200 лет назад. Но интересно же заглянуть за горизонт? И ученые уже предлагают совсем иные принципы работы источников питания для носимых нами гаджетов. Среди этих научных проектов – преобразование тепла человека в электричество с помощью стеклоткани, канализирование света с помощью фотоэлектрических органических ячеек, преобразование лактатов из человеческого пота в электричество с помощью «биотатуировки». Интересно, что же из этого выстрелит?
Коротко
Игорь Корнилов



 Роботы для дачи: освобождаемся от ненужной работы
Роботы для дачи: освобождаемся от ненужной работы  Головная роль
Головная роль Докопаться до воды
Докопаться до воды








