Доктор холод


Термин «рак» тоже ввел Гиппократ. Нет, о самой болезни знали и до него: в папирусе Эдвина Смита пятитысячелетней давности описано восемь случаев опухоли груди и применяемое в качестве лечения прижигание. А Геродот подробно описал течение болезни у Атоссы, жены персидского царя Дария. Болезнь была запущена, царица долгое время скрывала процесс, что позволило Геродоту упрекнуть ее в легкомыслии и составить трактат о необходимости выявлять заболевание на ранних стадиях. Но понять супругу Дария можно: выжигание как метод лечения было настолько мучительным, что пугало чуть ли не больше самой болезни.
На страницах своего труда «О карцинозе» Гиппократ тоже описал рак в запущенной стадии. Разросшееся в груди женщины новообразование было похоже на расплющенное членистоногое с клешнями из набухших кровеносных сосудов, питавших опухоль. «Кarkinos» – так обозначил заболевание Гиппократ, что и означает на греческом языке «рак».
Сегодня очень многие виды рака излечимы. Современные онкологи вводят пациента в долгосрочную ремиссию даже с метастазами в печени, хотя всего 20 лет назад это словосочетание звучало как смертный приговор. Единственное, что осталось за тысячелетия неизменным, это позднее обращение к врачам.
Почему я захотела написать эту статью? Потому что я знаю, что бояться не надо. Потому что среди моих подруг много тех, с кем я познакомилась в онкоклинике, и кто, пройдя курс лечения, живет полноценной жизнью. Потому что у меня метастаз в печени, но я даже не собираюсь сдаваться. И еще потому, что я своими глазами видела, как работают российские врачи, освоившие и внедрившие метод криоабляции. Приручив холод, хирурги используют его для лечения злокачественных и доброкачественных опухолей различных локализаций. И их работа дает многим людям шанс на жизнь.

Рассказывает Павел Балахнин, онколог, заведующий отделением рентгенохирургических методов диагностики и лечения Санкт-Петербургского клинического научно-практического центра специализированных видов медицинской помощи:
– Конечно, хирургическое лечение – это золотой стандарт в онкологии, но есть много состояний, когда по объективным обстоятельствам удалить опухоль хирургическим путем невозможно. Это может быть сопутствующая патология, определенная локализация образований или ограниченный резерв органа. Ну и достаточно много пациентов, у которых опухоль выявлена на поздней стадии, когда ее невозможно или крайне рискованно удалять именно хирургически.
Поэтому на протяжении тысяч лет многие врачи пытались воздействовать на опухоли физическим фактором: с помощью огня и льда, прижиганием и замораживанием. Но была проблема в том, что прижигать или замораживать получалось лишь те образования, которые человек видел, то есть опухоли наружных локализаций.
Сейчас для уничтожения опухолей применяется семь энергий: существует лазерная, ультразвуковая, радиочастотная, микроволновая абляции (от латинского ablatio – «отнятие»), криоабляция, фотодинамическая абляция и необратимая электропорация.
Все это изобреталось и внедрялось для применения в медицине вообще, а не только в онкологии. Например, использование радиочастотной энергии началось в электрохирургии – для разрезания тканей. Когда в середине XX века технический прогресс позволил перейти к эндоскопическим и лапароскопическим вмешательствам, то все эти энергии стали применяться и для лечения невидимых опухолей полых органов (к ним относится, например, желудок или мочевой пузырь). Воздействовать безопасно и эффективно на опухоли паренхиматозных органов (печени, почек, легких) было невозможно.
Но спустя время появились сначала экспериментальные, а затем и коммерчески доступные платформы, способные генерировать, передавать и локально использовать энергию для деструкции опухолей практически в любой точке организма.
И сегодня доступно клиническое использование этих технологий. Мы в нашей клинике работаем с тремя из них: радиочастотную, микроволновую и криоабляцию.
Все началось с радиочастотной абляции. Это самая технически простая методика, относительно недорогая, поэтому она быстро распространилась во всем мире. Но у нее есть ограничения, которые не позволяют создавать зоны некроза больше 5 см. А для уничтожения образований необходим так называемый край абляции: когда воздействие ведется не только на саму опухоль, но и на 5–10 мм здоровой ткани. То есть к большим опухолям эта технология применяться не может.
Более перспективна и надежна в этом плане микроволновая абляция, которая может увеличивать зоны деструкции до 8 см. И, конечно, криоабляция, которая позволяет создавать огромные ледяные шары – до 15 см. Но пока применение абляций ограничено размерами опухоли до 3 см, потому что помимо технологических возможностей есть и клинические рекомендации. И чтобы была оформлена новая рекомендация, должно пройти 10–15 лет применения методики.
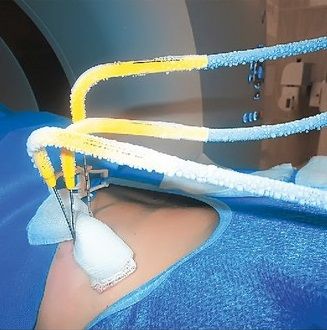
Вообще, использование отрицательных температур для лечения рака имеет длинную историю. В 1850 году впервые был применен замороженный солевой раствор для терапии опухолей молочной железы и тела матки. Только через век, в 1960-е, появились первые криогенные установки, работавшие на жидком азоте, позволившие провести серию опытов на животных. А в 1990-м была выпущена первая коммерчески доступная система, основанная на методе накачки азота, – криогенная установка второго поколения. При этом на протяжении всего XX века охлаждающее гипотермическое воздействие на опухоли было возможно только с использованием хирургических технологий. Появление же чрескожной криоабляции связано с созданием в начале 2000-х годов криогенных установок третьего поколения: в них для охлаждения криозондов используется не жидкий азот, а аргон, находящийся под большим давлением. Изменение технологии охлаждения криозондов позволило почти в десять раз уменьшить их диаметр. С этого момента и начались многочисленные исследования эффективности криоабляции для лечения опухолей печени, почек, легких, костей, надпочечников, молочных желез.
Около года назад в Санкт-Петербурге в клиническом научно-практическом центре специализированных видов медицинской помощи был введен в эксплуатацию аппарат SeedNet Gold (производства компании Galil Medical, США), предназначенный для криодеструкции опухолей. Петербург стал первым и пока единственным городом в России, где применяют криоабляцию для лечения именно злокачественных опухолей.
Опухоль при криоабляции подвергается очень быстрой и глубокой заморозке – до –40 °С, а потом производится такое же быстрое ее оттаивание.
Система для чрескожной криоабляции опухолей состоит из трех основных частей:
генерирующей установки (она вырабатывает энергию, имеет панель настроек и систему мониторинга процесса с помощью ультразвуковой аппаратуры), системы передачи энергии от генератора к аппликатору и, собственно, аппликатора – криозонда, который выполнен в виде длинной иглы. Небольшой укол или зуд в области ее введения – максимум, что испытывает пациент во время процедуры криоабляции.
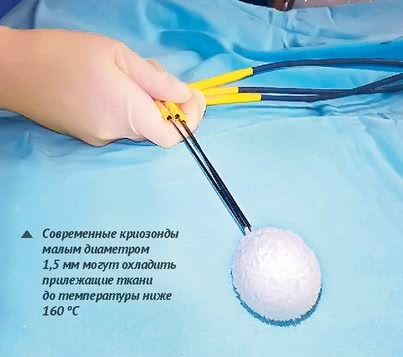
Принцип работы современных криогенных установок основан на эффекте Джоуля-Томсона – так называется изменение температуры газа при адиабатическом дросселировании – медленном протекании газа под действием постоянного перепада давлений сквозь дроссель (пористую перегородку). При проведении криоабляции аргон, находящийся под давлением в 240–300 атм., протекает по внутренней рабочей части криозонда в область пониженного давления через дроссельную заслонку – тонкий капилляр. Это приводит к его интенсивному охлаждению, передающемуся на стенки аппликатора. Интенсивное охлаждение – это и есть положительный эффект адиабатического дросселирования. Современные криозонды малым диаметром 1,5 мм могут охладить прилежащие ткани до температуры ниже 160 °С, а криозонды диаметром 2,1 мм – даже до температуры ниже 220 °C.
Потом за счет поглощения тепловой энергии происходит очень быстрое охлаждение окружающих тканей опухоли до критически низких температур в диапазоне от –20 до –40 °C. Это вызывает кристаллизацию внеклеточной и внутриклеточной жидкости, нарушение осмолярности клеток (суммы концентраций всех кинетически активных частиц. – Ред.) и затем их необратимое повреждение. Некротизированная опухоль не удаляется, а остается в организме человека in situ.
А для быстрого оттаивания криозонда используется гелий, обладающий, наоборот, не положительным, а отрицательным эффектом адиабатического дросселирования.
Очень важное преимущество криоабляции перед другими методами – это возможность создания иммунного ответа. Ведь главная опасность онкологического заболевания в том, что организм не распознает атипичные клетки, принимая злокачественные образования за «свои». А потому не уничтожает их, не запускает механизм апоптоза, позволяя раковой опухоли захватывать один орган за другим.
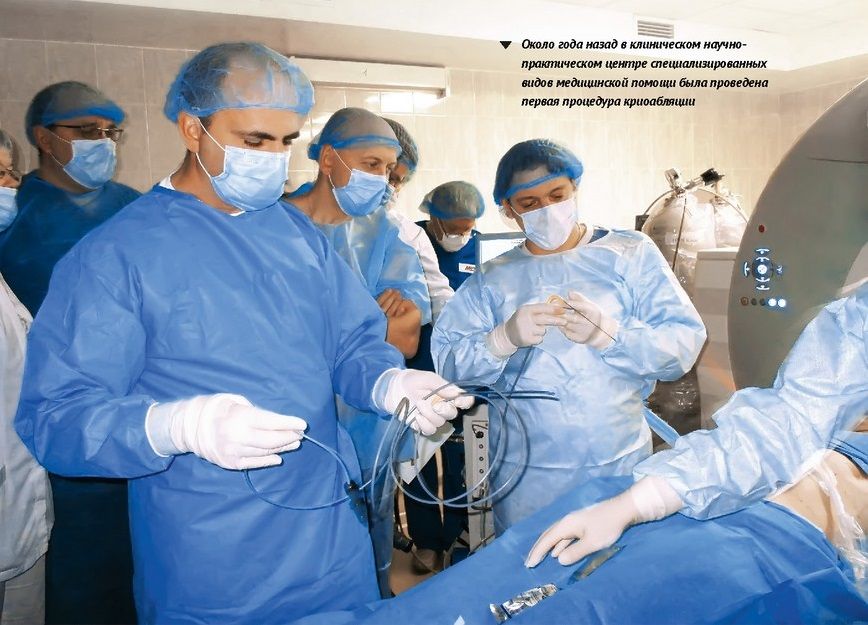
Павел Балахнин:
– При криоабляции работает механизм заморозки ткани, когда белки не разрушаются, а попадают в кровь, что вынуждает иммунную систему реагировать, распознавая эти белки. А если она распознает опухолевые антигены, то происходит стимуляция иммунного ответа, и возможно системное действие на весь организм после единичного локального вмешательства.
В литературе достаточно много наблюдений такого воздействия. Это называется «абскопальный эффект», исчезновение дистантных метастазов при онкотермическом воздействии на первичный очаг: когда одна опухоль подвергается абляции, а после этого начинают регрессировать метастазы в отдаленных органах.
На сегодняшний день это, наверное, самая интересная тема в хирургии. Врачи, работающие в этом направлении, стараются вычислить механизмы работы абляции и еще дополнительно воздействовать лекарственными препаратами, чтобы усилить этот эффект.
Освоенная петербургскими врачами технология начинает находить и другие области применения. Уже почти год в отделении рентгенохирургии проводят операции по удалению фиброаденом (доброкачественных опухолей груди) у женщин. Без разрезов, без тяжелого наркоза, без долгого восстановительного периода и без деформации молочной железы. И поездки в Израиль и Германию для такого врачебного вмешательства теперь не нужны.
Самое последнее из освоенного хирургами – это урологические операции по удалению аденомы простаты. И эта операция тоже требует только местного наркоза и в ведущих клиниках мира давно выведена из списка экспериментальных и поставлена на поток.
Излишний оптимизм нам, конечно, не нужен. От начала апробирования методики до массового ее внедрения всегда проходит время. Но надежда теперь действительно есть. А с надеждой всегда проще.
Наука
Вероника Севостьянова




 Бог из машины
Бог из машины Религия малых доз
Религия малых доз








